- 投稿邮箱:kxjscx@kxjscxzzs.com
- 在线编辑QQ:959914545
发布时间:2021-04-13 阅读数:424
杨健

摘? 要:前列地尔注射液设备清洁验证的目的是从目检、化学、微生物角度试验并证明前列地尔注射液生产线按规定的设备清洁SOP清洁后,使用小容量注射剂生产线生产产品时没有来自上批产品及清洁过程所带来污染的风险,从而保证了药品的安全、纯净和有效,并证明前列地尔注射液生产线的清洁SOP是有效可行的。该文主要分为两大部分:第一部分,对生产前列地尔注射液的配液系统、灌装系统等与药液直接接触的设备情况进行概述;第二部分,制定出设备清洁方案,然后根据设备清洁验证方案实施清洁验证,通过制定合格的清洁验证标准,选取适当的取样点进行验证,看是否在合格标准内。通过一系列的验证数据归纳分析,表明清洁验证结果的有效性、可靠性。
关键词:前列地尔注射液设备? 清洁方法? 清洁验证
中图分类号:R927.11 ? ?文献标识码:A 文章编号:1672-3791(2019)07(b)-0046-03
1? 生产前列地尔注射液的设备情况概述
前列地尔注射液为终端灭菌药品,在前列地尔注射液(规格:2mL:10μg)的生产过程中,与药品直接接触的设备主要有:配制系统(1号罐、2号罐、3号罐、4号罐、5号罐、管道、过滤系统)、灌封系统(贮药罐、分药罐、硅胶管、灌装针)。
其中配制系统、灌封系统(贮药罐)及连接管道按配液系统清洗SOP,采用在线清洗的方式进行清洗;灌装系统(分药罐、硅胶管、灌装针)按灌装机清洗SOP,灌装机采用手工清洗的方式。
因目前该生产线的配液系统(1号罐、2号罐、3号罐、4号罐、5号罐、管道、过滤系统)及灌封系统(贮药罐、分药罐、硅胶管、灌装针)为专用设备,只用于生产前列地尔注射液,化学残留量以最终洗涤水的电导率、pH值作为参考,不做化学最大残留量的计算,但清洁效果需考察最终淋洗水的pH值、电导率、微生物限度、细菌内毒素,以及擦拭取样检测微生物限度。
该验证要求3个生产连续批次进行清洁验证,清洁后对配液系统与灌装系统进行目检和残留检测,检测结果应全部合格,清洁验证方可通过。
2? 验证实施
2.1 验证计划
同步前列地尔注射液生产进行三批清洁验证。每批生产结束后按照各设备清洁SOP进行清洁,同时按照各設备清洁验证方案规定取样点进行取样检测。
2.2 取样工具、取样溶剂及取样方法
2.2.1 取样工具
带塞子锥形瓶250mL,带塞子无菌锥形瓶250mL,带塞子试管,带塞子无菌试管,普通棉签,无菌棉签。
2.2.2 取样溶剂
注射用水。
2.2.3 取样方法
(1)淋洗取样。
①在设备淋洗线路相对最下游处收集最终淋洗水,包括收集微生物测试样品和化学测试样品。
②取样完成后在试管上贴上标签,标明取样日期、样品编号及取样人。
(2)擦拭取样。
①擦拭表面的面积约为25cm2。
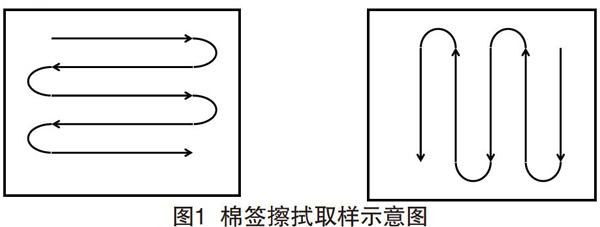
②用无菌棉签蘸取适当的注射用水对规定面积的设备表面进行擦拭取样。将棉签头按在取样表面上,用力使其弯曲,平稳而缓慢地擦拭取样表面,棉签擦拭取样图示意图见图1。
③取样完成后,将棉签用剪刀剪断,并放入试管并盖上。
④取样完成后在试管上贴上标签,标明取样日期、样品编号及取样人。
2.2.4 取样、测试
(1)按设备清洁验证取样计划的要求,准备好足够的取样工具。取样瓶需进行清洗、灭菌。
(2)在2017年11月进行的20171101、20171102、20171103三批前列地尔注射液生产完成后,按《配液系统清洁SOP》《灌装系统清洁SOP》进行清洁。
(3)清洁完成后,取最后一步淋洗水进行pH、电导率、微生物限度及内毒素测试,不破坏配液系统的密闭性,再对配液系统的表面进行目检,然后进行擦拭取样,考察微生物限度;灌装单元中的器具清洁完成后,取最后一步淋洗水进行pH、电导率、微生物限度及内毒素测试,并对设备表面进行目检,再对接液桶、过滤器滤筒进行擦拭取样,考察微生物限度。目检结果记录在表1中,pH值检测结果记录在表2中。
(4)依据设备清洁验证取样计划进行取样。
淋洗水样、擦拭样及其他样品按1.2描述的方法,用250mL的锥形瓶进行取淋洗水样。
(5)取样完成后在取样瓶上粘贴标签,标明样品名称、取样日期、样品编号及取样人等信息。
搅拌桨轴、搅拌桨内壁表面需全部取样。
管道连接处需对接口处及垫圈表面进行取样。
内毒素测试样品取样点用除热原的取样器取样。
(6)将样品送至化验室进行检测。
(7)检测完成后,将检测结果记录在表2、表3、表4中,并将检验报告作为方案的附件。
2.2.5 可接受标准
(1)目检。
按设备清洁规程清洁后,目检设备各表面应无可见残留物、异物,检测结果记录在表1的目检记录中。
(2)最终淋洗水样品。
最终淋洗水样品可接受标准见表5。
(3)擦拭样品。
擦试样品可接受标准见表2。
2.3 检验方法研究
微生物擦拭取样的回收率研究如下。
对微生物擦拭取样法的验证研究人员做了以下原因的分析:
⑴微生物是活的,会生长,在样品处理过程中某些微生物会死亡或者失去复活能力,因此取样无重复性。
⑵微生物擦拭不可能像化学残留那么容易达到均匀,因此擦拭的重复性非常差。
⑶擦拭本身会对菌株造成破坏。
⑷目前没有合适的对照菌种供选择。
⑸清洁验证中还同时取样考察淋洗水样的微生物限度。
综合以上几点因素,研究人员认为微生物擦拭取样的回收率研究没有意义,因此,没有对微生物擦拭取样方法进行验证。
2.4 验证结果的记录
前列地尔注射液设备清洁验证实施记录见表1、表2、表3、表4。
2.5? 验证数据分析及总结
根据《前列地尔注射液设备清洁验证方案》的要求,验证小组于2017年11月6~15日对小容量注射剂车间与前列地尔注射液药品接触的设备系统(包括配液系统、灌装系统)进行了连续3批清洁验证,验证过程所涉及前列地尔注射液生产批次包括:批号20171101、20171102、20171103。
验证结果及数据分析表明:按照批准的设备清洁SOP及清洁验证方案的规定要求进行清洁、取样及检测,清洗后淋洗水(或擦拭样品)的pH值、电导率、微生物限度及细菌内毒素均符合验证各项指标标准规定,清洁效果有效、清洁方法可靠。
参考文献
[1] 王艳敏.探讨注射用奥扎格雷钠设备清洁验证方法[J].科技创新导报,2014,11(12):200-203.
[2] 陈伙德,罗燕平,夏春森,等.冻干粉针剂配制灌装系统的清洁验证[J].中国医药工业杂志,2010,41(9):704-708.
[3] 黎阳.浅谈药品生产设备清洁验证[J].中国药事,2008(8):654-656.
编辑整理:科学技术创新杂志社编辑部 官方网站:www.hljkxzzs.com